- Yazar Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:52.
- Son düzenleme 2025-06-01 07:38.
Karbonik asit ve bikarbonat arasındaki temel fark, karbonik asidin nötr bir kimyasal bileşikken bikarbonatın negatif yüklü bir kimyasal bileşik olmasıdır.
Karbonik asit, H2CO3 kimyasal formülü ile karbondioksit suda çözündüğünde çözeltide oluşan zayıf bir asittir. Bikarbonat, üç oksijen atomu, bir hidrojen atomu ve bir karbon atomunun kimyasal formülü HCO3- ile birleşmesiyle oluşur.
Karbonik Asit Nedir?
Karbonik asit H2CO3'tür. Bazen bu ismi suda veya karbonatlı suda çözünmüş karbondioksit içeren çözeltilere veriyoruz. Bunun nedeni karbonatlı suyun az miktarda H2CO3 içermesidir. Ayrıca karbonik asit zayıf bir asittir ve karbonatlar ve bikarbonatlar olmak üzere iki tür tuz oluşturabilir. Bu bileşiğin molar kütlesi 62.024 g/mol'dür.
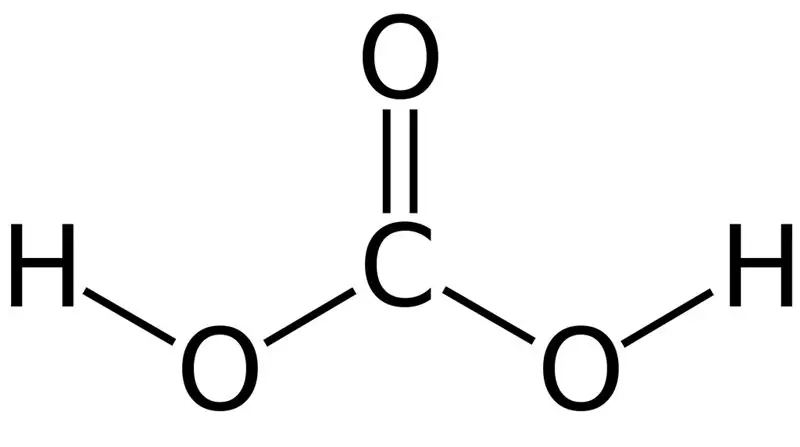
Şekil 01: Karbonik Asitin Kimyasal Yapısı
Karbondioksit suda çözündüğünde, karbondioksit ve karbonik asit arasında bir dengeye girer. Denge aşağıdaki gibidir:
CO2 + H2O ⟷ H2CO3
Bir baza fazla miktarda karbonik asit eklersek bikarbonat verir. Ancak, fazla miktarda baz varsa, karbonik asit karbonatlı tuzlar verme eğilimindedir. Daha kesin olarak, karbonik asit, karbonil karbonuna bağlı iki hidroksil grubu ikame edicisine sahip bir karboksilik asit bileşiğidir. Ayrıca, proton bağışlayabilen bir poliprotik asittir. Çıkarılabilir iki protonu vardır, bu nedenle özellikle diprotiktir.
Bikarbonat nedir?
Bikarbonat, üç oksijen atomu, bir hidrojen atomu ve bir karbon atomunun birleşimiyle oluşur. Bu kombinasyonun ürünü bir iyon veya protonlardan daha fazla elektrona sahip bir bileşik olabilir. HCO3-. kimyasal formülüne sahip kimyasal bir tür olarak tanımlayabiliriz.
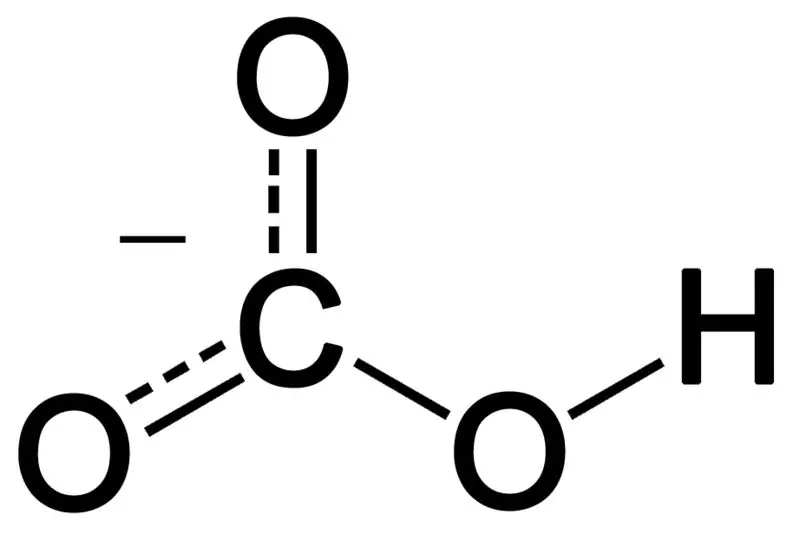
Şekil 02: Bikarbonat Anyonunun Kimyasal Yapısı
Bu bileşik, sıradan terimlerle vücudun pH tamponlama sisteminin çok önemli bir parçasıdır: kişinin kanını çok asidik veya çok bazik olmayan bir durumda tutmaktan sorumludur. Ek olarak, mide yiyecekleri sindirmeyi bitirdiğinde, sindirim sularını kontrol altında tutmanın bir yolu olarak hizmet eder. Ayrıca yağmur suyundaki karbonik asit, kayalara çarptığında bikarbonat iyonları oluşturur. Bu bikarbonat iyonları akışı, karbon döngüsünün devam etmesinde önemlidir.
Karbonik Asit ve Bikarbonat Arasındaki Fark Nedir?
Karbonik asit, karbondioksit suda çözündüğünde çözeltide oluşan zayıf bir asittir ve kimyasal formülü H2CO3'tür. Bikarbonat, kimyasal formülü HCO3- olan üç oksijen atomu, bir hidrojen atomu ve bir karbon atomunun bir araya gelmesiyle oluşur. temel fark karbonik asit ve bikarbonat arasında karbonik asit nötr bir kimyasal bileşik iken bikarbonat negatif yüklü bir kimyasal bileşiktir. Ayrıca karbonik asit, kabarcıklı, gazlı içecekler yapımında, derma titlerin tedavisinde, gargarada vb. kullanılırken, bikarbonat fırınlama gibi gıda müstahzarlarında (mayalama maddesi olarak) kullanılır ve pH'daki değişikliklere direnme yeteneği verir.
Aşağıdaki infografik, karbonik asit ve bikarbonat arasındaki farkı yan yana karşılaştırma için tablo biçiminde özetler.
Özet - Karbonik Asit ve Bikarbonat
Karbonik asit H2CO3'tür. Bikarbonat, HCO3- kimyasal formülü ile üç oksijen atomu, bir hidrojen atomu ve bir karbon atomunun bir araya gelmesiyle oluşur. Karbonik asit ve bikarbonat arasındaki temel fark, karbonik asidin nötr bir kimyasal bileşikken bikarbonatın negatif yüklü bir kimyasal bileşik olmasıdır.






